Эффективность применения экстракта плаценты человека для подкожного введения у пациентов с маточным фактором бесплодия в программах ВРТ
Введение
Несмотря на прогресс в медицине, проблема бесплодия по-прежнему остается актуальной. По данным метаанализа 2022 г., включившего более 32 исследований, распространенность бесплодия среди женского населения составила 46, % [1]. В РФ частота женского бесплодия составляет 17,2–24,0% [2]. Вспомогательные репродуктивные технологии (ВРТ): экстракорпоральное оплодотворение (ЭКО) и интрацитоплазматическая инъекция сперматозоидов (ИКСИ) являются эффективными методами лечения бесплодия [3]. Однако, несмотря на развитие ВРТ, актуальной проблемой остаются неудачи имплантации в программах ЭКО. Эффективность которых в среднем не превышает 40% [10]. Они могут быть связаны с различными причинами: иммунологическими, нарушениями микробиома полости матки и рецептивности эндометрия, анатомическими внутриматочными аномалиями или эмбриональным фактором [4]. Среди причин маточного бесплодия важную роль играет хронический эндометрит (ХЭ). Выявление маркера воспаления CD138 в полости матки (диагностического критерия ХЭ) является фактором, влияющим на снижение частоты наступления клинической беременности после переноса эмбриона [5]. Однако ХЭ часто протекает бессимптомно и, вероятно, недооценивается врачами. Взаимодействие бактерий с микроокружением эндометрия способствует изменениям в популяции лейкоцитов, выработке цитокинов и факторов роста, которые поддерживают негативное влияние на имплантационный потенциал эндометрия [6]. Согласно систематическому обзору 2022 г., ХЭ часто приводит к гипоплазии эндометрия (М-эхо <7 мм) и нарушению внутриматочной гемодинамики, что достоверно снижает частоту имплантации и нормального прогрессирования беременности [7]. Связь между ХЭ и неблагоприятными репродуктивными исходами подчеркивает необходимость комплексных диагностических и терапевтических стратегий для оптимизации результатов лечения бесплодия. Эффективный алгоритм лечения ХЭ включает физиотерапию [8], обладающую дефиброзирующим, трофикостимулирующим и вазоактивным действием и по показаниям антибактериальную терапию [9]. Предимплантационная диагностика эмбриона существенно повышает шансы на имплантацию – до 59%, особенно у группы пациенток старше 35 лет [10]. Стремление к дальнейшему повышению эффективности программ ЭКО приводит к поиску новых методов терапии. Так, проведенные исследования показали, что терапия препаратом «Мэлсмон», в основе которого лежит гидролизат плаценты человека, положительно влияет на состояние эндометрия, нормализуя функциональные параметры, значимые для реализации потенциала имплантации [11].
Целью данного исследования было оценить и обосновать результативность применения комплексного лечения, включающего пептидную терапию, у пациенток с хроническим эндометритом, ассоциированных в программы ВРТ.
Материалы и методы
Набор материала осуществляли в Клиническом госпитале «Лапино» Группы компаний «Мать и дитя» с 2015 по декабрь 2024 г. с соблюдением этических требований и оформлением информированного добровольного согласия.
Материал исследования составили 129 пациенток репродуктивного возраста, средний возраст 36±1,22 года. Критерии включения: бесплодие маточного генеза (N97.2) и подтвержденный диагноз «хронический эндометрит» (СD 138+) (N71.1); наличие в накоплении одного и более эуплоидных эмбрионов, рекомендованных к переносу после проведенного предимплантационного тестирования. Критерии исключения: гинекологические заболевания, требующие хирургического лечения; экстрагенитальные заболевания в стадии декомпенсации; онкологические заболевания; противопоказания к ВРТ, физиотерапии и пептидной терапии.
Задачей первого этапа было получение эуплоидного эмбриона. Пациенткам проводили забор ооцитов (в естественном цикле или в протоколе со стимуляцией овуляции), выполняли культивирование эмбрионов, их предимплантационное генетическое тестирование (ПГТ-А) и криоконсервацию. Вторым этапом пациенткам проводили биопсию эндометрия в средней фазе пролиферации (8–11-й дни менструального цикла) с последующим морфологическим и молекулярным исследованием, включая оценку биоценоза полости матки. Диагноз ХЭ верифицировался при выявлении лимфоплазмоцитарной инфильтрации эндометрия (CD 138+). Кроме того, до начала лечения, на 5–7-й день после овуляции оценивали величину М-эхо и структуру эндометрия, внутриматочную гемодинамику с помощью эходопплерометрии.
На следующем этапе, с 5–7-го дня цикла, пациентки получали классическую аппаратную физиотерапию ХЭ. При наличии показаний в цикле физиотерапии была проведена антибактериальная терапия с учетом результатов исследования биоценоза полости матки. Пациенткам рекомендовали барьерную контрацепцию в течение месяца, в котором производилась физиотерапия, а также в следующем после лечения цикле (цикле «покоя»).
В следующем после физиолечения менструальном цикле повторно проводили сонографическое и допплерометрическое исследования, оценивали динамику жалоб. К переносу эмбрионов допускали женщин с М-эхо более 7,5 мм и нормальными показателями внутриматочной перфузии.
Далее пациентки случайным образом были разделены на две группы. У женщин I группы (n=76) в третьем или последующем цикле, но не позднее 6 месяцев был проведен криоперенос эуплоидного эмбриона, прошедшего ПГТ. В цикле переноса эмбриона пациентам подкожно, в область живота вводили 6,0 мл гидролизата плаценты «Мэлсмон»: 5 введений, с 3–5-го дня менструального цикла, через 1–2 дня. Введение препарата заканчивалось не позднее чем за 2 дня до переноса эмбриона. Пациенткам II группы (n=53) криопереносу эуплоидного эмбриона не предшествовала пептидная терапия.
Эффективность переноса эмбриона оценивали по динамике показателей ХГЧ в плазме крови, начиная с 10–12-го дня после криопереноса. На 21-й день с помощью ультразвукового исследования подтверждали наличие плодного яйца в полости матки, а через 36 дней определяли визуализацию эмбриона и сердцебиения. Далее уточняли исходы беременности на основании медицинской документации.
Систематизацию полученных данных производили в Microsoft Office Excel 2021. Статистическая обработка выполнена с помощью программы IBM SPSS Statistica, версия 22 (IBM Corporation, США). Соответствие данных нормальному распределению определяли с помощью критерия Колмогорова–Смирнова. Для показателей, характеризующих качественные признаки, указывали абсолютное число (n) и относительную величину (%). Различия качественных признаков анализировали при помощи χ2-критерия. Осуществляли расчет среднеарифметических и среднеквадратичных отклонений. Для сравнения между группами исследования использовали t-критерий Стьюдента. Критическим уровнем значимости считали различия при p<0,05.
Результаты исследования
Всего было обследовано 129 пациенток. Женщины были рандомно разделены на две группы, сопоставимые по основным социальным, анамнестическим (акушерский и гинекологический анамнез) и клиническим показателям (гинекологические и соматические заболевания).
Учитывая однородность двух групп, проведенный анализ жалоб, анамнеза, обследований не имел статистически значимой разницы.
Ведущей жалобой пациенток обеих групп было отсутствие наступления беременности. Первичное бесплодие составляло 38,3% в I группе и 40,5% – во II группе, вторичное – 61,7 и 59,5% (p>0,05) соответственно. В прошлом имели 1 и более неудачных переносов эмбрионов в I группе 19,3% и во II группе – 2,5% (p>0,05). Изменение менструальной кровопотери в виде гипоменореи наблюдалось у 32,7% в I группе и 29,4% – во II группе (p>0,05), межменструальные мажущие кровяные выделения беспокоили 17,3 и 19,5% соответственно (p>0,05). 33,4% в I группе и 35,2% во II группе предъявляли жалобы на альгодисменорею (p>0,05). Глубокая диспареуния беспокоила 37,7 и 36,9% соответственно (p>0,05).
По данным акушерско-гинекологического анамнеза: невынашивание беременности в прошлом имели 23,1% в I группе и 22,6% – во II группе (p>0,05); хирургический аборт – 16,4 и 15,2% соответственно (p>0,05); внематочную беременность – 9,2% в I и 9,8% – во II группе (p>0,05).
Воспалительные заболевания органов малого таза в анамнезе наблюдались у 40,1% в I группе и 39,4% во II группе (p>0,05). При этом распространенность внутриматочных синехий составила 9,6 и 10,3% соответственно (p>0,05).
Анализ внутриматочных вмешательств показал: частота раздельного диагностического выскабливания по поводу патологии эндометрия в анамнезе составила 49,2 и 53,5% (p>0,05); хирургических абортов – 16,4% в I группе и 15,2 % – во II группе (p>0,05); повторное выскабливание полости матки после аборта или выкидыша по поводу остатков плодного яйца составило соответственно 7,8 и 7,3% (p>0,05); наличие в анамнезе внутриматочной системы в полости матки – 5,6 и 5,9% (p>0,05).
При сонографическом исследовании средняя толщина М-эхо составляла 8,1± 0,73 мм в I группе и 8,3± 0,8 мм во II группе (p>0,05). Толщина М-эхо меньше 7,5 мм наблюдалась у 27,3%, «экстремально тонкий» эндометрий (менее 5 мм) – у 8,2% женщин. Трехслойная однородная структура эндометрия наблюдалась у 37,% в I группе и 38,1 % – во II группе (p>0,05).
Анализ оценки внутриматочной гемодинамики, проведенный с помощью допплерометрического исследования, показал у пациенток с ХЭ в двух группах гиповаскуляризацию эндометрия, несимметричность перфузии, изменение углонезависимых индексов (PI, RI) преимущественно на уровне радиальных, базальных и спиральных артерий. Только в 30,2% в I группе и 32,9% во II группе удавалось визуализировать спиральные артерии (p>0,05)
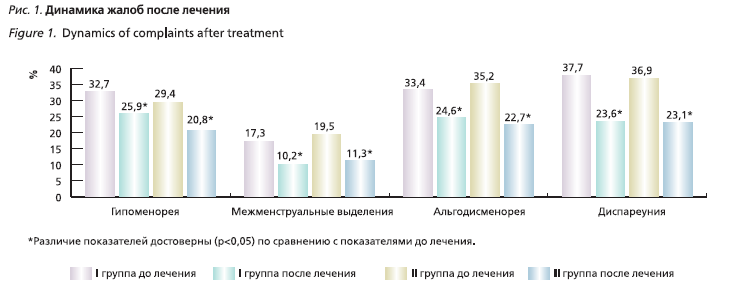
После проведенного лечения в обеих группах пациентки отметили увеличение менструальной кровопотери, отсутствие межменструальных мажущих выделений, уменьшение болевого синдрома при менструации, уменьшение боли при половом контакте (рис. 1).
При ультразвуковой оценке состояния эндометрия в период «окна имплантации» после физиолечения выявлены следующие изменения: увеличение толщины М-эхо составило 9,5±0,42 мм в I группе и 9,73±0,37 мм –во II группе (р <0,05). Трехслойная однородная структура эндометрия выявлена у 73,9% I группе и 74,9% – во II группе (p <0,05).
По данным допплерометрического исследования, у 87,5% в I группе и у 89,2% во II группе (p <0,05) отмечалось улучшение параметров субэндометриального кровотока. Визуализация спиральных артерий увеличилась и составила 68,7 и 71,2% соответственно (р <0,05) (таблица).
.png)
В соответствии с дизайном исследования, криоперенос эмбрионов был проведен только пациенткам с величиной М-эхо >7,5 мм и нормальными показателями внутриматочной гемодинамики. У пациенток I группы (n=76), где криопереносу эмбрионов предшествовала «Mэлсмон»-терапия, частота наступления беременности составила 73% (56 пациенток). На момент окончания исследования: прогрессирующую беременность наблюдали у 9 человек, роды живым ребенком – у 41 женщины, неразвивающаяся беременность – у 5 человек, антенатальная гибель плода – 1. Во II группе (n=53) беременность наступила у 35 женщин, что составило 66%: прогрессирующая – у 19 пациенток, роды живым ребенком – у 14 женщин, неразвивающаяся беременность – у 2.
Необходимо отметить, что у всех пациенток, получавших плацентарную терапию, отсутствовали осложнения, требующие отмены препарата. Однако у некоторых женщин (11%) отмечены такие нежелательные явления, как появление незначительных гематом в месте введения.
Обсуждение результатов
Эндометрий играет важнейшую роль в реализации репродуктивной функции, поддерживая адгезию бластоцисты, инвазию трофобласта и развитие плода. ХЭ привлекает внимание из-за его связи с неблагоприятными репродуктивными исходами (повторные потери беременности, повторные неудачи имплантации и бесплодие) [12]. При хроническом воспалении в эндометрии определяются повышение уровня цитотоксичных клеток и Т-лимфоцитов, возрастает содержание провоспалительных цитокинов, меняется экспрессия фактора некроза опухоли, маркера пролиферации Ki-67, стероидных рецепторов, усиливаются явления апоптоза. В совокупности эти изменения приводят к нарушению рецептивности в ткани [8, 13]. Меняется архитектоника эндометрия за счет развития инфильтративных и склеротических процессов [14], что ведет к гипоплазии эндометрия. Тонкий эндометрий в «окне имплантации» связан с неблагоприятными исходами беременности у женщин после ЭКО/ИКСИ.
По данным метаанализа, включающего 22 публикации, наблюдалась тенденция к снижению показателей исходов беременности (коэффициента живорождения, частоты клинической беременности и частоты имплантации) [15]. Учитывая вышеизложенные данные, диагностика ХЭ, включая определение маркеров воспаления и микробиома полости матки, является важным этапом прегравидарной подготовки [16]. Основным методом лечения ХЭ считается назначение антибактериальной терапии [9]. Однако в России традиционно широко используют назначение физических факторов. Морфологические и иммуногистохимические исследования показали, что физиотерапия уменьшает экспрессию макрофагов, коллагена III и IV типа, эпидермальных и трансформирующих факторов роста в эндометрии и нормализует рецептивность эндометрия [8, 17]. Исследования многих авторов и собственный опыт показывают, что физиотерапия усиливает внутриматочный кровоток, увеличивает исходно сниженную васкуляризацию стромы эндометрия и миометрия [17, 18]. Так, в нашем исследовании толщина эндометрия у пациенток в обеих группах выросла в среднем в 1,2 раза, улучшилась внутриматочная гемодинамика: частота визуализации концевых артерий матки в среднем составила 70% против 30%; восстановилась симметричность кровотока в миометрии, снизился индекс резистентности. Это подтверждает эффективность использования комбинации антибактериальной терапии и физических факторов для достижения не только противомикробного эффекта, но и восстановления структурной и сосудистой архитектоники эндометрия.
Диагностика хронического эндометрита и его лечение как этап прегравидарной подготовки, несомненно, повышает шансы на успешную имплантацию. Однако в возрастной группе пациенток старше 35 лет значимую роль начинает играть эмбриональный фактор неудач. Хромосомные аномалии являются причиной 50–70% выкидышей на сроке менее 10 недель в общей репродуктивной популяции [19]. Частота анеуплоидий к 43 годам составляет около 85% [20]. Согласно систематическому обзору 2023 г., беременность в результате ЭКО с ПГТ-А имела значительно более высокую частоту имплантации, частоту клинической беременности, частоту живорождений и значительно более низкую частоту клинических выкидышей. Так, клиническая беременность была диагностирована у 59% женщин, против 40% – при ЭКО/ИКСИ без генетического тестирования [10]. В наше исследование вошли исключительно женщины, имеющие в накоплении эмбрионы после ПГТ-А, т.е. исключающие эмбриональный фактор неудач.
Несмотря на вышеизложенные факты, актуальной задачей врачей во всем мире остается поиск методов, повышающих эффективность ВРТ. Появляется все больше публикаций о применении мононуклеарных клеток периферической крови, аутоплазменной терапии, гранулоцитарного колониестимулирующего фактора, метаболической терапии и прочее.
Одним из средств, влияющих на клеточной метаболизм, является пептидный препарат «Мэлсмон» (гидролизат плаценты человека). «Мэлсмон» зарегистрирован на территории Российской Федерации в 2011 г. как рецептурный препарат для подкожного введения. Показание – коррекция астенических состояний у женщин в пери- и постменопаузе [21]. В Японии этот препарат производится с 1956 г. Эффективность и безопасность применения ГПЧ у женщин в перименопаузе доказана в большом количестве зарубежных [22–24], а также выполненных на территории Российской Федерации исследований [25, 26]. Известно,
что в основе механизмов лечебного действия препарата «Мэлсмон» лежит способность увеличивать энергетический потенциал клеток, причем ведущую роль играет модуляция митохондриальной функции. Оптимизация активности клеток обусловлена тенденцией к стабилизации клеточных мембран, нормализации функциональной активности митохондрий, синтеза нуклеиновых кислот и белков [27].
Положительное влияние гидролизата плаценты человека на эндометрий показано в наших более ранних исследованиях [28] и публикациях других авторов [29, 30]. Большой интерес представляет исследование, проведенное проф. Кветным И.М., где на культуре клеток эндометрия было продемонстрировано статистически достоверное увеличение экспрессии важнейших сигнальных молекул (кальретикулина, кисспептина и сиртуина-1), обеспечивающих рецептивность эндометрия под воздействием препарата «Мэлсмон» [11]. Эти данные свидетельствуют о повышении восприимчивости эндометрия к имплантации и патогенетически обосновывают его применение у пациентов в циклах ВРТ, особенно при наличии факторов, снижающих потенциал имплантации, таких как ХЭ. Согласно полученным в
нашем исследовании результатам, применение препарата «Мэлсмон» как заключительный этап подготовки к криопереносу эмбриона вносит определенный вклад в конечный результат и демонстрирует тенденцию к повышению частоты наступления беременности. Так, эффективность криопереноса эмбриона после ЭКО, по данным литературы, даже при ПГТ-А составляет 59% [10]. По нашим данным, ЭКО с ПГТ-А и предварительной физиотерапевтической подготовкой эндометрия привела к повышению частоты имплантации до 66%, а при дополнении данного лечения «Мэлсмон»-терапией – до 73% (рис. 2).
.png)
Следует отметить высокий уровень производственного процесса при создании препарата «Мэлсмон», в ходе которого в составе остаются исключительно низкомолекулярные соединения – аминокислотные остатки белков с молекулярной массой 1-3 кДА. Таким образом, препарат не содержит гормонов, факторов роста, ферментов и витаминов. Кроме того, этап ультрананофильтрации обеспечивает низкую
иммуногенность и стандартизованный состав, что дополнительно обусловливает безопасность его использования, продемонстрированную в нашем исследовании.
Заключение
Выявлена отчетливая тенденция к повышению частоты наступления беременности в группе комплексного лечения, включающего пептидную терапию, по сравнению с пациентами, у которых введение препарата «Мэлсмон» не проводилось.
Подготовка к криопереносу эмбриона, включающая морфологические и молекулярные методы диагностики состояния эндометрия, комплексную терапию хронического эндометрита, предимплантационное генетическое тестирование эмбрионов и «Мэлсмон»-терапию в фертильном цикле, привела к высокой частоте наступления беременности в изучаемой группе. Так, частота наступления беременности после
комплексного лечения составила 73%, что выше приведенных в научной литературе данных. Применение гидролизата плаценты человека «Мэлсмон», по-видимому, вносит определенный вклад в достигнутый результат, поскольку отсутствие данного этапа подготовки при полной идентичности предшествующего лечения сопровождалось менее высоким результатом преодоления бесплодия в программах ВРТ.
.png)
.png)
Несмотря на прогресс в медицине, проблема бесплодия по-прежнему остается актуальной. По данным метаанализа 2022 г., включившего более 32 исследований, распространенность бесплодия среди женского населения составила 46, % [1]. В РФ частота женского бесплодия составляет 17,2–24,0% [2]. Вспомогательные репродуктивные технологии (ВРТ): экстракорпоральное оплодотворение (ЭКО) и интрацитоплазматическая инъекция сперматозоидов (ИКСИ) являются эффективными методами лечения бесплодия [3]. Однако, несмотря на развитие ВРТ, актуальной проблемой остаются неудачи имплантации в программах ЭКО. Эффективность которых в среднем не превышает 40% [10]. Они могут быть связаны с различными причинами: иммунологическими, нарушениями микробиома полости матки и рецептивности эндометрия, анатомическими внутриматочными аномалиями или эмбриональным фактором [4]. Среди причин маточного бесплодия важную роль играет хронический эндометрит (ХЭ). Выявление маркера воспаления CD138 в полости матки (диагностического критерия ХЭ) является фактором, влияющим на снижение частоты наступления клинической беременности после переноса эмбриона [5]. Однако ХЭ часто протекает бессимптомно и, вероятно, недооценивается врачами. Взаимодействие бактерий с микроокружением эндометрия способствует изменениям в популяции лейкоцитов, выработке цитокинов и факторов роста, которые поддерживают негативное влияние на имплантационный потенциал эндометрия [6]. Согласно систематическому обзору 2022 г., ХЭ часто приводит к гипоплазии эндометрия (М-эхо <7 мм) и нарушению внутриматочной гемодинамики, что достоверно снижает частоту имплантации и нормального прогрессирования беременности [7]. Связь между ХЭ и неблагоприятными репродуктивными исходами подчеркивает необходимость комплексных диагностических и терапевтических стратегий для оптимизации результатов лечения бесплодия. Эффективный алгоритм лечения ХЭ включает физиотерапию [8], обладающую дефиброзирующим, трофикостимулирующим и вазоактивным действием и по показаниям антибактериальную терапию [9]. Предимплантационная диагностика эмбриона существенно повышает шансы на имплантацию – до 59%, особенно у группы пациенток старше 35 лет [10]. Стремление к дальнейшему повышению эффективности программ ЭКО приводит к поиску новых методов терапии. Так, проведенные исследования показали, что терапия препаратом «Мэлсмон», в основе которого лежит гидролизат плаценты человека, положительно влияет на состояние эндометрия, нормализуя функциональные параметры, значимые для реализации потенциала имплантации [11].
Целью данного исследования было оценить и обосновать результативность применения комплексного лечения, включающего пептидную терапию, у пациенток с хроническим эндометритом, ассоциированных в программы ВРТ.
Материалы и методы
Набор материала осуществляли в Клиническом госпитале «Лапино» Группы компаний «Мать и дитя» с 2015 по декабрь 2024 г. с соблюдением этических требований и оформлением информированного добровольного согласия.
Материал исследования составили 129 пациенток репродуктивного возраста, средний возраст 36±1,22 года. Критерии включения: бесплодие маточного генеза (N97.2) и подтвержденный диагноз «хронический эндометрит» (СD 138+) (N71.1); наличие в накоплении одного и более эуплоидных эмбрионов, рекомендованных к переносу после проведенного предимплантационного тестирования. Критерии исключения: гинекологические заболевания, требующие хирургического лечения; экстрагенитальные заболевания в стадии декомпенсации; онкологические заболевания; противопоказания к ВРТ, физиотерапии и пептидной терапии.
Задачей первого этапа было получение эуплоидного эмбриона. Пациенткам проводили забор ооцитов (в естественном цикле или в протоколе со стимуляцией овуляции), выполняли культивирование эмбрионов, их предимплантационное генетическое тестирование (ПГТ-А) и криоконсервацию. Вторым этапом пациенткам проводили биопсию эндометрия в средней фазе пролиферации (8–11-й дни менструального цикла) с последующим морфологическим и молекулярным исследованием, включая оценку биоценоза полости матки. Диагноз ХЭ верифицировался при выявлении лимфоплазмоцитарной инфильтрации эндометрия (CD 138+). Кроме того, до начала лечения, на 5–7-й день после овуляции оценивали величину М-эхо и структуру эндометрия, внутриматочную гемодинамику с помощью эходопплерометрии.
На следующем этапе, с 5–7-го дня цикла, пациентки получали классическую аппаратную физиотерапию ХЭ. При наличии показаний в цикле физиотерапии была проведена антибактериальная терапия с учетом результатов исследования биоценоза полости матки. Пациенткам рекомендовали барьерную контрацепцию в течение месяца, в котором производилась физиотерапия, а также в следующем после лечения цикле (цикле «покоя»).
В следующем после физиолечения менструальном цикле повторно проводили сонографическое и допплерометрическое исследования, оценивали динамику жалоб. К переносу эмбрионов допускали женщин с М-эхо более 7,5 мм и нормальными показателями внутриматочной перфузии.
Далее пациентки случайным образом были разделены на две группы. У женщин I группы (n=76) в третьем или последующем цикле, но не позднее 6 месяцев был проведен криоперенос эуплоидного эмбриона, прошедшего ПГТ. В цикле переноса эмбриона пациентам подкожно, в область живота вводили 6,0 мл гидролизата плаценты «Мэлсмон»: 5 введений, с 3–5-го дня менструального цикла, через 1–2 дня. Введение препарата заканчивалось не позднее чем за 2 дня до переноса эмбриона. Пациенткам II группы (n=53) криопереносу эуплоидного эмбриона не предшествовала пептидная терапия.
Эффективность переноса эмбриона оценивали по динамике показателей ХГЧ в плазме крови, начиная с 10–12-го дня после криопереноса. На 21-й день с помощью ультразвукового исследования подтверждали наличие плодного яйца в полости матки, а через 36 дней определяли визуализацию эмбриона и сердцебиения. Далее уточняли исходы беременности на основании медицинской документации.
Систематизацию полученных данных производили в Microsoft Office Excel 2021. Статистическая обработка выполнена с помощью программы IBM SPSS Statistica, версия 22 (IBM Corporation, США). Соответствие данных нормальному распределению определяли с помощью критерия Колмогорова–Смирнова. Для показателей, характеризующих качественные признаки, указывали абсолютное число (n) и относительную величину (%). Различия качественных признаков анализировали при помощи χ2-критерия. Осуществляли расчет среднеарифметических и среднеквадратичных отклонений. Для сравнения между группами исследования использовали t-критерий Стьюдента. Критическим уровнем значимости считали различия при p<0,05.
Результаты исследования
Всего было обследовано 129 пациенток. Женщины были рандомно разделены на две группы, сопоставимые по основным социальным, анамнестическим (акушерский и гинекологический анамнез) и клиническим показателям (гинекологические и соматические заболевания).
Учитывая однородность двух групп, проведенный анализ жалоб, анамнеза, обследований не имел статистически значимой разницы.
Ведущей жалобой пациенток обеих групп было отсутствие наступления беременности. Первичное бесплодие составляло 38,3% в I группе и 40,5% – во II группе, вторичное – 61,7 и 59,5% (p>0,05) соответственно. В прошлом имели 1 и более неудачных переносов эмбрионов в I группе 19,3% и во II группе – 2,5% (p>0,05). Изменение менструальной кровопотери в виде гипоменореи наблюдалось у 32,7% в I группе и 29,4% – во II группе (p>0,05), межменструальные мажущие кровяные выделения беспокоили 17,3 и 19,5% соответственно (p>0,05). 33,4% в I группе и 35,2% во II группе предъявляли жалобы на альгодисменорею (p>0,05). Глубокая диспареуния беспокоила 37,7 и 36,9% соответственно (p>0,05).
По данным акушерско-гинекологического анамнеза: невынашивание беременности в прошлом имели 23,1% в I группе и 22,6% – во II группе (p>0,05); хирургический аборт – 16,4 и 15,2% соответственно (p>0,05); внематочную беременность – 9,2% в I и 9,8% – во II группе (p>0,05).
Воспалительные заболевания органов малого таза в анамнезе наблюдались у 40,1% в I группе и 39,4% во II группе (p>0,05). При этом распространенность внутриматочных синехий составила 9,6 и 10,3% соответственно (p>0,05).
Анализ внутриматочных вмешательств показал: частота раздельного диагностического выскабливания по поводу патологии эндометрия в анамнезе составила 49,2 и 53,5% (p>0,05); хирургических абортов – 16,4% в I группе и 15,2 % – во II группе (p>0,05); повторное выскабливание полости матки после аборта или выкидыша по поводу остатков плодного яйца составило соответственно 7,8 и 7,3% (p>0,05); наличие в анамнезе внутриматочной системы в полости матки – 5,6 и 5,9% (p>0,05).
При сонографическом исследовании средняя толщина М-эхо составляла 8,1± 0,73 мм в I группе и 8,3± 0,8 мм во II группе (p>0,05). Толщина М-эхо меньше 7,5 мм наблюдалась у 27,3%, «экстремально тонкий» эндометрий (менее 5 мм) – у 8,2% женщин. Трехслойная однородная структура эндометрия наблюдалась у 37,% в I группе и 38,1 % – во II группе (p>0,05).
Анализ оценки внутриматочной гемодинамики, проведенный с помощью допплерометрического исследования, показал у пациенток с ХЭ в двух группах гиповаскуляризацию эндометрия, несимметричность перфузии, изменение углонезависимых индексов (PI, RI) преимущественно на уровне радиальных, базальных и спиральных артерий. Только в 30,2% в I группе и 32,9% во II группе удавалось визуализировать спиральные артерии (p>0,05)
После проведенного лечения в обеих группах пациентки отметили увеличение менструальной кровопотери, отсутствие межменструальных мажущих выделений, уменьшение болевого синдрома при менструации, уменьшение боли при половом контакте (рис. 1).
При ультразвуковой оценке состояния эндометрия в период «окна имплантации» после физиолечения выявлены следующие изменения: увеличение толщины М-эхо составило 9,5±0,42 мм в I группе и 9,73±0,37 мм –во II группе (р <0,05). Трехслойная однородная структура эндометрия выявлена у 73,9% I группе и 74,9% – во II группе (p <0,05).

По данным допплерометрического исследования, у 87,5% в I группе и у 89,2% во II группе (p <0,05) отмечалось улучшение параметров субэндометриального кровотока. Визуализация спиральных артерий увеличилась и составила 68,7 и 71,2% соответственно (р <0,05) (таблица).
.png)
В соответствии с дизайном исследования, криоперенос эмбрионов был проведен только пациенткам с величиной М-эхо >7,5 мм и нормальными показателями внутриматочной гемодинамики. У пациенток I группы (n=76), где криопереносу эмбрионов предшествовала «Mэлсмон»-терапия, частота наступления беременности составила 73% (56 пациенток). На момент окончания исследования: прогрессирующую беременность наблюдали у 9 человек, роды живым ребенком – у 41 женщины, неразвивающаяся беременность – у 5 человек, антенатальная гибель плода – 1. Во II группе (n=53) беременность наступила у 35 женщин, что составило 66%: прогрессирующая – у 19 пациенток, роды живым ребенком – у 14 женщин, неразвивающаяся беременность – у 2.
Необходимо отметить, что у всех пациенток, получавших плацентарную терапию, отсутствовали осложнения, требующие отмены препарата. Однако у некоторых женщин (11%) отмечены такие нежелательные явления, как появление незначительных гематом в месте введения.
Обсуждение результатов
Эндометрий играет важнейшую роль в реализации репродуктивной функции, поддерживая адгезию бластоцисты, инвазию трофобласта и развитие плода. ХЭ привлекает внимание из-за его связи с неблагоприятными репродуктивными исходами (повторные потери беременности, повторные неудачи имплантации и бесплодие) [12]. При хроническом воспалении в эндометрии определяются повышение уровня цитотоксичных клеток и Т-лимфоцитов, возрастает содержание провоспалительных цитокинов, меняется экспрессия фактора некроза опухоли, маркера пролиферации Ki-67, стероидных рецепторов, усиливаются явления апоптоза. В совокупности эти изменения приводят к нарушению рецептивности в ткани [8, 13]. Меняется архитектоника эндометрия за счет развития инфильтративных и склеротических процессов [14], что ведет к гипоплазии эндометрия. Тонкий эндометрий в «окне имплантации» связан с неблагоприятными исходами беременности у женщин после ЭКО/ИКСИ.
По данным метаанализа, включающего 22 публикации, наблюдалась тенденция к снижению показателей исходов беременности (коэффициента живорождения, частоты клинической беременности и частоты имплантации) [15]. Учитывая вышеизложенные данные, диагностика ХЭ, включая определение маркеров воспаления и микробиома полости матки, является важным этапом прегравидарной подготовки [16]. Основным методом лечения ХЭ считается назначение антибактериальной терапии [9]. Однако в России традиционно широко используют назначение физических факторов. Морфологические и иммуногистохимические исследования показали, что физиотерапия уменьшает экспрессию макрофагов, коллагена III и IV типа, эпидермальных и трансформирующих факторов роста в эндометрии и нормализует рецептивность эндометрия [8, 17]. Исследования многих авторов и собственный опыт показывают, что физиотерапия усиливает внутриматочный кровоток, увеличивает исходно сниженную васкуляризацию стромы эндометрия и миометрия [17, 18]. Так, в нашем исследовании толщина эндометрия у пациенток в обеих группах выросла в среднем в 1,2 раза, улучшилась внутриматочная гемодинамика: частота визуализации концевых артерий матки в среднем составила 70% против 30%; восстановилась симметричность кровотока в миометрии, снизился индекс резистентности. Это подтверждает эффективность использования комбинации антибактериальной терапии и физических факторов для достижения не только противомикробного эффекта, но и восстановления структурной и сосудистой архитектоники эндометрия.
Диагностика хронического эндометрита и его лечение как этап прегравидарной подготовки, несомненно, повышает шансы на успешную имплантацию. Однако в возрастной группе пациенток старше 35 лет значимую роль начинает играть эмбриональный фактор неудач. Хромосомные аномалии являются причиной 50–70% выкидышей на сроке менее 10 недель в общей репродуктивной популяции [19]. Частота анеуплоидий к 43 годам составляет около 85% [20]. Согласно систематическому обзору 2023 г., беременность в результате ЭКО с ПГТ-А имела значительно более высокую частоту имплантации, частоту клинической беременности, частоту живорождений и значительно более низкую частоту клинических выкидышей. Так, клиническая беременность была диагностирована у 59% женщин, против 40% – при ЭКО/ИКСИ без генетического тестирования [10]. В наше исследование вошли исключительно женщины, имеющие в накоплении эмбрионы после ПГТ-А, т.е. исключающие эмбриональный фактор неудач.
Несмотря на вышеизложенные факты, актуальной задачей врачей во всем мире остается поиск методов, повышающих эффективность ВРТ. Появляется все больше публикаций о применении мононуклеарных клеток периферической крови, аутоплазменной терапии, гранулоцитарного колониестимулирующего фактора, метаболической терапии и прочее.
Одним из средств, влияющих на клеточной метаболизм, является пептидный препарат «Мэлсмон» (гидролизат плаценты человека). «Мэлсмон» зарегистрирован на территории Российской Федерации в 2011 г. как рецептурный препарат для подкожного введения. Показание – коррекция астенических состояний у женщин в пери- и постменопаузе [21]. В Японии этот препарат производится с 1956 г. Эффективность и безопасность применения ГПЧ у женщин в перименопаузе доказана в большом количестве зарубежных [22–24], а также выполненных на территории Российской Федерации исследований [25, 26]. Известно,
что в основе механизмов лечебного действия препарата «Мэлсмон» лежит способность увеличивать энергетический потенциал клеток, причем ведущую роль играет модуляция митохондриальной функции. Оптимизация активности клеток обусловлена тенденцией к стабилизации клеточных мембран, нормализации функциональной активности митохондрий, синтеза нуклеиновых кислот и белков [27].
Положительное влияние гидролизата плаценты человека на эндометрий показано в наших более ранних исследованиях [28] и публикациях других авторов [29, 30]. Большой интерес представляет исследование, проведенное проф. Кветным И.М., где на культуре клеток эндометрия было продемонстрировано статистически достоверное увеличение экспрессии важнейших сигнальных молекул (кальретикулина, кисспептина и сиртуина-1), обеспечивающих рецептивность эндометрия под воздействием препарата «Мэлсмон» [11]. Эти данные свидетельствуют о повышении восприимчивости эндометрия к имплантации и патогенетически обосновывают его применение у пациентов в циклах ВРТ, особенно при наличии факторов, снижающих потенциал имплантации, таких как ХЭ. Согласно полученным в
нашем исследовании результатам, применение препарата «Мэлсмон» как заключительный этап подготовки к криопереносу эмбриона вносит определенный вклад в конечный результат и демонстрирует тенденцию к повышению частоты наступления беременности. Так, эффективность криопереноса эмбриона после ЭКО, по данным литературы, даже при ПГТ-А составляет 59% [10]. По нашим данным, ЭКО с ПГТ-А и предварительной физиотерапевтической подготовкой эндометрия привела к повышению частоты имплантации до 66%, а при дополнении данного лечения «Мэлсмон»-терапией – до 73% (рис. 2).
.png)
Следует отметить высокий уровень производственного процесса при создании препарата «Мэлсмон», в ходе которого в составе остаются исключительно низкомолекулярные соединения – аминокислотные остатки белков с молекулярной массой 1-3 кДА. Таким образом, препарат не содержит гормонов, факторов роста, ферментов и витаминов. Кроме того, этап ультрананофильтрации обеспечивает низкую
иммуногенность и стандартизованный состав, что дополнительно обусловливает безопасность его использования, продемонстрированную в нашем исследовании.
Заключение
Выявлена отчетливая тенденция к повышению частоты наступления беременности в группе комплексного лечения, включающего пептидную терапию, по сравнению с пациентами, у которых введение препарата «Мэлсмон» не проводилось.
Подготовка к криопереносу эмбриона, включающая морфологические и молекулярные методы диагностики состояния эндометрия, комплексную терапию хронического эндометрита, предимплантационное генетическое тестирование эмбрионов и «Мэлсмон»-терапию в фертильном цикле, привела к высокой частоте наступления беременности в изучаемой группе. Так, частота наступления беременности после
комплексного лечения составила 73%, что выше приведенных в научной литературе данных. Применение гидролизата плаценты человека «Мэлсмон», по-видимому, вносит определенный вклад в достигнутый результат, поскольку отсутствие данного этапа подготовки при полной идентичности предшествующего лечения сопровождалось менее высоким результатом преодоления бесплодия в программах ВРТ.
.png)
.png)

