Аллогенный препарат плаценты Мэлсмон®: современные возможности замедления старения кожи
Авторы:
Кветной Игорь Моисеевич, Заслуженный деятель науки РФ, профессор, доктор медицинских наук
Полякова Виктория Олеговна, Профессор РАН, доктор биологических наук, профессор НИИ акушерства, гинекологии и репродуктологии им. Д.О. Отта, Санкт-Петербургский институт биорегуляции и геронтологии, Санкт-Петербургский государственный университет
Палькова Галина Борисовна, врач-дерматовенеролог, косметолог, эндокринолог клиники современных технологий «Триактив», Москва
Абстракт
Плацента человека содержит широкий спектр биологически активных веществ, способных оказывать выраженное действие на процессы обновления и регенерации тканей. Лабораторные исследования показывают повышение маркеров клеточного обновления и регенерации в культуре фибробластов под воздействием стандартизированного препарата плаценты Мэлсмон®, что свидетельствует о его геропротекторных свойствах по отношению к клеткам кожи человека.
Ключевые слова: препарат плаценты, Мэлсмон, геропротекторы, фибробласты
Геропротекторы — движение против времени, но по законам биологииКлеточное старение заключается в необратимой остановке клеточного цикла в ответ на разнообразные внутренние и внешние неблагоприятные факторы. В отличие от гамет и стволовых клеток, подавляющее большинство соматических клеток человека окончательно прекращают делиться по прохождении характерного для данной культуры клеток числа клеточных делений и вступают в стабильное состояние ареста клеточного цикла, именуемое клеточным (или репликативным) старением. При этом стареющие клетки сохраняют жизнеспособность и метаболическую активность, осуществляя секрецию множества факторов, которые позже были объединены в название «старческий секреторный фенотип» (SASP; от англ. senescence associated secretory phenotype). SASP включает в себя различные провоспалительные цитокины, хемокины, ростовые факторы и протеазы [1–3]. Показано, что через секрецию данных факторов стареющие клетки способны оказывать влияние на свое микроокружение, в том числе воздействовать на процессы пролиферации, дифференцировки и выживания соседних клеток. Одним из основных компонентов секреторного фенотипа, ассоциированного со старением, является продукция провоспалительных цитокинов, в частности интерлейкина-6 (ИЛ-6) и -8 (ИЛ-8). Известно, что ИЛ-6 является цитокином широкого спектра действия и способен регулировать процессы пролиферации, дифференцировки, а также выживания клеток. ИЛ-8 хорошо известен как фактор хемотаксиса нейтрофилов, но в качестве его клеточных мишеней могут выступать и эндотелиальные клетки, миграция и пролиферация которых определяют эффективность процессов неоангиогенеза. Одной гранью действия SASP являются участие в процессе эмбрионального развития, активация процессов регенерации и репарации тканей, антиканцерогенное действие. С другой стороны, накопление стареющих клеток, вызванное нарушением их элиминации иммунной системой, ведет к повышению уровня секретируемых ими провоспалительных цитокинов, что приводит к хроническому воспалительному процессу, сопровождающемуся фиброзом и клеточной дисфункцией (рис. 1). Данный процесс в долгосрочной перспективе способствует развитию таких возрастассоциированных заболеваний, как остеоартрит, болезнь Альцгеймера, фиброз легких и др., и состояний, таких как возрастные изменения кожи (атрофия кожной ткани, морщины, купероз, нарушение пигментации).
Стареющие клетки, с одной стороны, воздействуют на свое микроокружение посредством секретируемых ими сигнальных молекул, с другой — сами могут послужить мишенью для препаратов на основе биологически активных веществ.
Группа веществ, способных снижать скорость возрастных изменений тканей и тем самым увеличивать продолжительность жизни и препятствовать развитию возраст-ассоциированных заболеваний, получила название геропротекторы. Среди них выделяют три основных категории [2] (рис. 2):
- геромодуляторы — замедляют процесс клеточного старения или способствуют морфологическим и функциональным преобразованиям постаревших клеток (их «омоложению»), блокируют SASP;
- геромедиаторы — активируют удаление постаревших клеток иммунной системой;
- сенолитики — избирательно инициируют гибель постаревших клеток.
В международной базе геропротекторов содержится информация о 259 веществах, испытанных по меньшей мере на 13 живых организмах — от дрожжеподобных грибов до человека [4]. Наряду с поиском новых веществ-геропротекторов и изучением механизмов их действия актуальными являются такие направления, как:
- разработка технологий производства коммерческих продуктов с клинически подтвержденной геропротекторной эффективностью;
- расширение спектра показаний для уже известных препаратов в сторону профилактики возраст-ассоциированных изменений в организме.
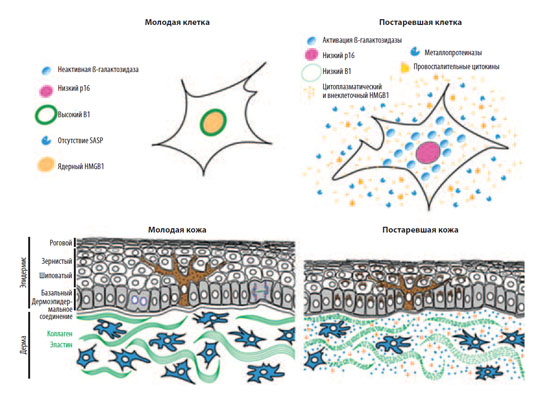
Рис. 1. Схематическое представление молодой и постаревшей кожи Возрастные изменения клеток кожи (верхняя половина рисунка): увеличение и уплощение клеток, повышение активности ß-галактозидазы, повышение экспрессии p16, снижение экспрессии белка ядерной пластинки В1, транслокация HMGB1 в цитоплазму и внеклеточное пространство, секреция факторов SASP. Особенности кожи с признаками старения (нижняя половина рисунка): истончение кожи за счет нарушения пролиферации и атрофических изменений, нарушение пигментации (коричневым отмечен меланоцит), уменьшение численности фибробластов (отмечены голубым), разрушение коллагеновых волокон, повышение концентрации провоспалительных факторов в межклеточном пространстве [3].

Рис. 2. Механизмы действия различных групп геропротекторов на постаревшие клетки [2]
Плацентарная терапия: биологическое обоснование, клинические эффекты и возможности применения
Вещества, выполняющие сигнальные функции, путешествуют по организму от секретирующей их клетки к клетке-мишени. Эти клетки могут быть расположены друг от друга на значительном расстоянии, и в этом случае мы имеем дело с эндокринной регуляцией организма, а сигнальные вещества называем гормонами. Или же они могут быть соседями в рамках одного органа (ткани), и тогда мы говорим о межклеточной коммуникации с помощью местных цитокинов (паракринная регуляция). Вне зависимости от расстояния, на которое передаются сигнальные вещества, они небольшого размера и растворимы в воде, чтобы иметь возможность переноситься кровью и диффундировать в межклеточной жидкости. И есть еще один важный момент: многие сигнальные вещества универсальны для организмов — представителей одного царства. Например, один и тот же цитокин выполняет одинаковые функции у разных млекопитающих и не имеет видоспецифичности. Чем ближе родство донора и реципиента, тем выше сходство полученной от донора композиции цитокинов с той, которая характерна для реципиента, и тем более выраженным будет результат ее применения. В этом и заключается суть так называемой тканевой терапии, когда в качестве лекарственного препарата используется препарат, полученный из ткани (органа) животного. Плазма крови и межклеточная жидкость любого органа насыщены различными сигнальными веществами и могут быть источником для их получения [5–8]. Но все-таки наибольшая концентрация цитокинов в сочетании с веществами, необходимыми для метаболизма, наблюдается именно в плаценте. Причем в силу функциональной специфики в плаценте особенно много веществ, которые контролируют процессы деления и дифференцировки клеток, лежащих в основе роста и репарации. Это обстоятельство (наряду с возможностью использования для масштабного производства плаценты человека) делает плаценту практически идеальным источником для получения препаратов как с восстановительными и заживляющими свойствами, так и с геропротекторным эффектом.

Рис. 3. Применяемые в клинической практике биоматериалы, полученные из плаценты [10]
Компоненты плаценты (плацента, пуповина, амниотические оболочки) заинтересовали ученых в качестве источника стволовых клеток и биологически активных веществ в конце ХХ в. (рис. 3, 4), хотя история плацентотерапии началась гораздо раньше [8–12]. Первое упоминание плаценты в качестве лекарственного средства встречается в руководстве по лекарственным средствам «Бэньцао ганму», написанном в XVI веке китайским биологом и фармацевтом Ли Шичженем , где ее лечебным свойствам посвящен целый раздел. Метод плацентарной терапии был предложен основателем Института глазных болезней и тканевой терапии профессором В.П. Филатовым в 1933 г. В зависимости от решаемых задач препараты плаценты могут вводиться непосредственно в кровь, инъецироваться в кожу и подкожные слои или же наноситься местно. Препараты плаценты обладают широким спектром полезных эффектов, среди которых противовоспалительный, обезболивающий, цито- и радиозащитный, противоаллергический, заживляющий. В основе этих эффектов лежат такие механизмы, как снижение уровня свободных радикалов и провоспалительных цитокинов (например, ИЛ-6, ФНО, ИЛ-1), стимуляция процессов пролиферации и репарации [11], нормализация тканевого гомеостаза и клеточного метаболизма. Плацентотерапия успешно применяется в разных сферах медицины, в большей степени — в хирургии, неврологии, гинекологии и дерматологии. Особо выраженных клинических эффектов удалось достичь при использовании плацентарной терапии для лечения ран, длительно незаживающих язв, ожогов: наблюдалось ускорение эпителизации и ангиогенеза, уменьшение отечности тканей и болевого синдрома. Предположительно, ранозаживляющее действие обусловлено повышением фактора роста фибробластов в начальной стадии регенерации и VEGF (фактор роста эндотелия сосудов) в поздней фазе.

Рис. 4. Морфология плацентарных компонентов: А, Б — плацентарная ткань (Тр — трофобласт; Cс — сосуды, Мез — мезенхима); В — зародышевые оболочки (Ам — амнион, Хр — хорион); Г — поверхностные клетки эпителия амниона; Д — пуповина на срезе; Е — ткань пуповины [10]
Применение препаратов плаценты в гинекологии при менопаузальных расстройствах позволяет нормализовать гормональный профиль, снизить выраженность «приливов» и раздражительность. В проведенных исследованиях наблюдалось уменьшение тяжести вагинальной атрофии как следствие повышения количества рецепторов к эстрогенам, активизация остеобластов. Плацентарная терапия тревожных расстройств позволяла добиться снижения тревожности и повышения стрессоустойчивости; предположительно, в основе достигнутого эффекта лежат подъем уровня внутриклеточного кальция, активация Т-клеток и спленоцитов, редукция синтеза провоспалительных цитокинов, ассоциированных с тревожными расстройствами (ИЛ-6, ФНО, γ-ИФН). В неврологии применение плацентарных экстрактов способствовало регенерации нервной ткани за счет активации синтеза факторов регенерации (GAP-43, Cdc2) [11]. Но все это относится к лечению уже имеющихся у пациента заболеваний. С развитием превентивной медицины фокус все больше сдвигается на профилактику различных состояний и патологий, в том числе возраст-ассоциированных. И в этом плане плацентотерапия оказалась очень эффективной благодаря способности индуцировать морфологические и функциональные преобразования постаревших клеток, тем самым «омолаживая» их и препятствуя секреции SASP.
Препарат Мэлсмон® — высокоочищенный гидролизат плаценты
Компании-производители вкладывают большие усилия и средства в то, чтобы отладить процесс производства продукта, стандартизированного по составу и имеющего доказанную эффективность. Стандартизация означает, что в готовых к использованию препаратах биологически активные вещества присутствуют в необходимой концентрации и в оптимальных пропорциях, а цельные клетки, гормоны, химические реагенты и балластные вещества отсутствуют. Кроме этого, стандартизация предполагает соблюдение на каждом этапе всех необходимых технологических шагов, что гарантирует наличие заявленных свойств (терапевтическая активность, срок годности) у препаратов из разных партий. Коммерческие препараты плаценты отличаются друг от друга по составу и свойствам, и это понятно, поскольку технологии их получения будут различными. Один из самых популярных плацентарных препаратов, имеющих международное признание, — препарат Мэлсмон® (Melsmon), представляющий собой высокоочищенный гидролизат плаценты человека. Препарат был разработан в 1950-х гг. в Японии на базе Токийского университета по госзаказу с целью помощи пострадавшим от ядерного взрыва. За многие годы технология получения препарата отточена до совершенства, и сегодня на всех этапах производства — от забора биоматериала до его фасовки — соблюдаются международные правила GMP, гарантирующие высокий уровень безопасности и эффективности готового продукта [8–10].
1-й этап. Отбор и заготовка человеческой плаценты
Специально разработанная система безопасности при заготовке биологического материала одобрена органами здравоохранения Японии и гарантирует блокировку распространения инфекции. Для получения «чистого» плацентарного материала по контрактам с медицинскими учреждениями отслеживаются беременные женщины, не имеющие инфекционных заболеваний. Кандидаты неоднократно проходят исследования на СПИД, гепатит В, гепатит С и другие заболевания. Сразу после родов плацента замораживается на определенный период в отдельном герметичном пластиковом пакете.
2-й этап. Экстракция, гидролиз и очистка
В производстве препарата Мэлсмон® не используют центральную часть плаценты и пуповину, в которых содержится большое количество гормонов и строма, а только высокоактивную часть плаценты — терминальные ворсинки хориона. Сырье очищают методом молекулярного фракционирования от высокомолекулярных белков, гормонов, бактерий, вирусов, прионов и других потенциально опасных компонентов. Исключительная безопасность препарата обеспечивается благодаря использованию фильтров 4-го поколения. В процессе производства используют запатентованный производителем экстрагент (растворитель), а не традиционные фенол или спирт. Биологический материал нагревают в соляной кислоте при температуре 100 °С от 15 до 17 ч, благодаря процессам расщепления и транспирации ткань плаценты переходит в водорастворимое состояние. Затем соляную кислоту выпаривают, а ее остаточные количества нейтрализуют с помощью гидроксида натрия до pH крови (6,8–7,0). При этом происходит гидролиз и денатурирование белков, но сохраняются важные плацентарные биоактивные компоненты размером до 5,5 кДа — аминокислоты и низкомолекулярные пептиды, нуклеотиды и малые фрагменты нуклеиновых кислот, минеральные вещества и др.
3-й этап. Стабилизация и стерилизация
Стабильные свойства препарата Мэлсмон® на весь срок годности обеспечивает бензиловый спирт в концентрации 12–18 мг/мл. Помимо консервирующего эффекта, бензиловый спирт создает внутрикожное депо для медленного физиологического распределения биологически активных веществ, а также оказывает обезболивающее действие. Конечный продукт помещают в стерильную ампулу. В каждой ампуле (2 мл) содержится 100 мг активнодействующей природной смеси. Ампулы с препаратом подвергают окончательной стерилизации под высоким давлением и при температуре 120 °С в автоклаве в течение 30 мин, что позволяет достичь высокого уровня биологической безопасности. В Японии препарат Мэлсмон® зарегистрирован в 1956 г. и уже более 60 лет входит в объем общественного обязательного медицинского страхования для лечения климакса и гипогалактии. В России препарат получил регистрационное свидетельство лекарственного средства в 2011 г. и был разрешен для применения в медицинских целях.
Состав и биологические свойства препарата Мэлсмон®
Аллогенный плацентарный препарат Мэлсмон® содержит различные биомолекулы плаценты, обладающие широким диапазоном биологических эффектов. В его составе:
- низкомолекулярные пептиды — осуществляют котрансляционный или посттрансляционный транспорт белка в соответствующую органеллу (ядро, митохондрия, хлоропласт, эндоплазматический ретикулум, апопласт или пероксисома) и таким образом влияют на экспрессию генов, создают оптимальный физиологический темп деления клеток, регулируют межклеточные взаимодействия и нормализуют метаболические процессы [10];
- аминокислоты (в том числе незаменимые) — регулируют процессы биосинтеза белка, которые с возрастом нарушаются (тирозин, триптофан, фенилаланин, урацил), а также нейтрализуют свободные радикалы (глютаминовая, аспарагиновая аминокислоты);
- полидезоксирибонуклеотиды — фрагменты молекулы ДНК высокой степени очистки активируют синтез собственной ДНК клетки, усиливают клеточную пролиферацию, стимулируют синтез коллагена;
- моносахариды — восстанавливают перекисное окисление липидов (антиоксидантное действие), активизируют противовоспалительные процессы;
- полиненасыщенные жирные кислоты — выполняют пластическую, энергетическую, а также регуляторную функции;
- макро- и микроэлементы —принимают участие в различных метаболических и дыхательных биохимических путях в клетках, в том числе в роли коферментов.
Изучение регуляторных свойств препарата Мэлсмон® посредством современных методов молекулярной диагностики позволяет рассматривать препарат в качестве потенциального биорегулятора метаболических и физиологических процессов в различных органах и тканях. В экспериментальном исследовании in vitro было установлено, что в основе механизма действия препарата Мэлсмон® лежит его способность усиливать энергетический потенциал клеток, способствуя нормализации функциональной активности митохондрий. По мнению авторов, это приводит к оптимизации клеточного обмена, тем самым тормозится формирование и прогрессирование патологических процессов как на клеточном уровне, так и организме в целом [9, 10].
Исследование влияния биологически активных компонентов препарата Мэлсмон® на старение фибробластов кожи человека
Кветной и соавт. провели оценку возможности применения препарата Мэлсмон® в качестве регуляторного и геропротекторного средства для профилактики старения кожи фибробластов человека in vitro [13].
| Таблица 1. Функции исследуемых маркеров [13] | |
| Маркер | Функции маркера |
| Ki-67 | Фактор пролиферации, присутствует в ядрах всех делящихся клеток, является информативным показателем для определения интенсивности деления фибробластов кожи |
| Кальретикулин (CALR) | Маркер эндоплазматической сети (ЭПС), является шопероном, в комплексе с кальнексином принимает участие в формировании третичной структуры белков, контролирует поток белков и гликопротеинов от ЭПС к аппарату Гольджи, не давая неправильно свернутым молекулам перемещаться в цис-зону аппарата Гольджи, обеспечивает регуляцию внутриклеточной концентрации кальция, связывая активными центрами молекулы кальция и удерживая их |
| Синтаксин-6 (STX6) | Маркер аппарата Гольджи, принимает участие в транспорте белков, в фибробластах человека регулирует пост-Гольджи транспорт и доставку компонентов микродоменов мембраны, таких как ганглиозид GM1 (гликосфинголипид) и кавеолин-1, в плазматическую мембрану. Кавеолин-1 участвует в образовании кавеол, которые, в свою очередь, опосредуют мембранный транспорт, эндоцитоз и формирование клеточного ответа на внешний сигнал. Также STX6 необходим для ретроградного переноса в транс-полюс аппарата Гольджи гликосфинголипидов, ассоциированных с мембранными микродоменами, и холестерина, полученного из липопротеинов низкой плотности |
| Сиртуин-6 (SIRT6) | Регулятор транскрипции и стабильности генома, теломерной целостности, репарации ДНК и метаболического гомеостаза, играет важную роль в регуляции процессов репарации ДНК. SIRT6 способствует репарации двунитевых разрывов ДНК через дополнительные механизмы, стимулируя резекцию ДНК при рекомбинационной репарации разрывов ДНК (HDR) и активации поли-АДФ-рибозилтрансферазы PARP-1 |
| Сиртуин-1 (SIRT1) | Экспрессируется в ядрах клеток всех органов, предположительно является одним из факторов, определяющих продолжительность жизни у млекопитающих. Участвует в различных клеточных процессах, в том числе репрессии транскрипции в ответ на стресс, ремоделировании хроматина, регуляции и дифференцировке клеток, активации метаболических путей |
| Фактор индукции апоптоза (AIF) | Митохондриальный проапоптозный белок, запускает путь апоптоза, независимый от каспаз, вызывая конденсацию хроматина и фрагментацию ДНК в клетке. Уровень AIF повышается при старении клетки |
| Таблица 2. Изменение экспрессии маркеров клеточной регенерации в культуре фибробластов человека на 3-м и 14-м пассажах с препаратом Мэлсмон® по сравнению с контролем (без препарата Мэлсмон®) (*p < 0,05) [13] | ||||||
| Маркер | Относительная площадь экспрессии сигнальных молекул, % | |||||
| Контроль | 3-й пассаж (молодые клетки) | Относительное изменение экспрессии под воздействием Мэлсмон® | Контроль | 14-й пассаж (старые клетки) | Относительное изменение экспрессии под воздействием Мэлсмон® | |
| Ki-67 | 1,50 | 2,82* | 1,88 | 1,11 | 1,84* | 1,66 |
| Кальретикулин | 10,22 | 15,46* | 1,51 | 6,42 | 9,84 | 1,53 |
| Сиртуин-1 | 3,88 | 5,06 | 1,30 | 1,01 | 2,15* | 2,13 |
| Сиртуин-6 | 0,59 | 1,16* | 1,97 | 0,34 | 0,85* | 2,50 |
| Синтаксин-6 | 4,39 | 5,38* | 1,23 | 3,15 | 3,42 | 1,09 |
| AIF | 1,56 | 1,94 | 1,24 | 6,55 | 4,06 | 0,62 |

Рис. 5. Экспрессия SIRT-1 в культуре клеток фибробластов, иммунофлуоресцентная конфокальная микроскопия, ×400. Для окрашивания ядер использовали Hoechst 33258 (синяя флуоресценция). Визуализацию SIRT-1 проводили с помощью вторичных антител, конъюгированных с Alexa Fluor 555 (желтая флуоресценция): после введения препарата Мэлсмон® желтое свечение становится заметным (красные стрелки) [13]
Материалы и методы
Источником культуры клеток фибробластов (n = 3) послужила нормальная пуповина человека, полученная при естественных срочных родах на 40-й неделе беременности. Пассирование клеток проводилось через 3 дня на 4-й по достижении культурой состояния монослоя. Клетки культивировались до 3-го (молодая культура) и 14-го пассажей (старая культура). Все культуры фибробластов были разделены на две группы:
- контрольная — культура фибробластов человека с введением физиологического раствора;
- тестовая — культура фибробластов человека с введением препарата Мэлсмон® (200 мкл на 3 мл питательной среды).
В качестве показателей геропротекторного эффекта были выбраны сигнальные молекулы, наиболее активно участвующие в механизмах клеточного обновления и регенерации — Ki-67, сиртуин-1 (Sirt1), сиртуин-6 (Sirt6), кальретикулин (CALR), синтаксин-6 (STX6), а также AIF (табл. 1). Для изучения экспрессии сигнальных молекул и структурно-функциональной организации клеточных культур фибробластов использовались молекулярно-морфологические методы: иммуноцитохимическое маркирование, иммунофлуоресцентная конфокальная лазерная сканирующая микроскопия, морфометрия, 3D-реконструкция, компьютерный анализ микроскопических изображений. Зеленая и красная флуоресценция отражали экспрессию исследуемых маркеров. Площадь экспрессии рассчитывалась как отношение площади, занимаемой иммунопозитивными клетками, к общей площади клеток в поле зрения для маркеров с цитоплазма тическим окрашиванием и как отношение площади, занимаемой иммунопозитивными ядрами, к общей площади ядер в поле зрения для маркеров с ядерной экспрессией. Показатели площади экспрессии выражали в процентах.
Результаты
При оценке экспрессии основных маркеров клеточной регенерации в молодой (3-й пассаж) и старой (14-й пассаж) культурах фибробластов человека было установлено увеличение показателей экспрессии маркеров под воздействием препарата Мэлсмон® (табл. 2, рис. 5). И хотя относительное изменение экспрессии маркеров, показывающее, во сколько раз экспрессия меняется, у культур молодых и старых клеток отличались, общая тенденция к повышению экспрессии при добавлении Мэлсмон® очевидна. Что касается фактора, индуцирующего апоптоз (AIF), то в данном исследовании не было выявлено статистически достоверных отличий между контрольной и тестовой группами ни в молодой, ни в старой культуре, что служит аргументом в пользу безопасности препарата Мэлсмон®.
Выводы
- Старение сопровождается уменьшением экспрессии Ki-67 в фибробластах и других клетках. Увеличение данного показателя под действием препарата Мэлсмон® как в молодой, так и в старой культурах свидетельствует об активной пролиферации фибробластов, что in vivo отражает активную регенерацию ткани.
- Снижение с возрастом содержания кальретикулина приводит к нарушению контроля качества белка, что влечет за собой деструктивные изменения. В присутствии препарата Мэлсмон® в клеточной культуре наблюдается усиление синтетической активности фибробластов человека, что подтверждается увеличением площади экспрессии кальретикулина и синтаксина-6 в группах с введением препарата.
- Активация экспрессии белков семейства сиртуинов под воздействием препарата Мэлсмон® обусловливает стабильность генома, защиту клеток от преждевременного старения и обеспечивает выполнение клетками биологических функций.
- Препарат Мэлсмон® не воздействует на апоптоз в культурах клеток.
Таким образом, применение препарата Мэлсмон® при старении культуры клеток фибробластов позволяет добиться увеличения показателей экспрессии сигнальных молекул-модуляторов клеточного обновления и регенерации до аналогичных в молодой культуре, что отражает его геропротекторное действие, обеспечивающее защиту ДНК от повреждений и стабильность генома, давая клетке возможность дольше выполнять запрограммированные функции. Это позволяет использовать препарат в качестве средства, стимулирующего регенераторные процессы в коже и препятствующего ее старению.
Заключение
Чем старше пациент, тем выше вероятность получения недостаточного результата или даже нежелательной реакции. Это связано с тем, что в коже нарастают воспалительный, окислительный и метаболический стрессы, и на этом фоне восприимчивость клеток к косметологическим воздействиям меняется. Биологический препарат Мэлсмон® обладает 100% биодоступностью и моментально включается в метаболические процессы, нормализуя и стабилизируя гомеостаз. Именно поэтому препарат может быть рекомендован прежде всего «сложным» пациентам со сниженным регенераторным потенциалом, с признаками раннего старения. При работе с такими пациентами применение препарата Мэлсмон® позволит снизить риск нежелательных явлений и осложнений, сократить период реабилитации и добиться более выраженного и стойкого результата. Доказательные геропротекторные свойства препарата позволяют рекомендовать препарат Мэлсмон® как основу современных протоколов профилактики и «замедления» старения, а сочетанное применение с эстетическими процедурами обеспечит желаемый результат как для врача, так и для пациента.
Литература
- Рамазанов Б.Р., Бойчук С.В., Ризванов А.А. Особенности ассоциированного со старением секреторного фенотипа гастроинтестинальных опухолей (ГИСТ). Гены & клетки 2014; IX(3): 173–178.
- Kim E-C., Kim J-R. Senotherapeutics: emerging strategy for healthy aging and age-related disease. BMB Rep 2019; 52(1): 47–55.
- Wang A.S., Dreesen O. Biomarkers of Cellular Senescence and Skin Aging. Front Genet 2018; 9: 247.
- http://geroprotectors.org
- Villeda S.A., Plambeck K.E., Middeldorp J., Castellano J.M., Mosher K.I., Luo J., Smith L.K., Bieri G., Lin K., Berdnik D., Wabl R., Udeochu J., Wheatley E.G., Zou B., Simmons D.A., Xie X.S., Longo F.M., Wyss-Coray T. Young blood reverses age-related impairments in cognitive function and synaptic plasticity in mice. Nature Med 2014; 20: 659–663.
- Conese M., Carbone A., Beccia E., Angiolillo A. The Fountain of Youth: A Tale of Parabiosis, Stem Cells, and Rejuvenation. Open Med (Wars) 2017; 12: 376–383.
- Castellano J.M., Mosher K.I., Abbey R.J. Human umbilical cord plasma prote ins revitalize hippocampal function in aged mice. Nature 2017; 544: 488–492.
- Измайлова Т.Д. Персонализированные протоколы метаболической коррекции как основа anti-age программ. Инъекционные методы в косметологии 2016; 1: 24–37.
- Измайлова Т.Д. Персонализированная PRP-терапия. Алгоритм подготовки пациента. Инъекционные методы в косметологии 2016; 2: 19–23.
- Палькова Г.Б. Перименопауза и возрастные изменения кожи: современный подход к ведению пациентов. Инъекционные методы в косметологии 2016; 3: 44–52.
- Pogozhykh O., Prokopyuk V., Figueiredo C., Pogozhykh D. Placenta and Placental Derivatives in Regenerative Therapies: Experimental Studies, History, and Prospects. Stem Cells Int 2018; 2018: 4837930.
- Silini A.R., Cargnoni A., Magatti M., Pianta S., Parolini O. The Long Path of Human Placenta, and Its Derivatives, in Regenerative Medicine. Front Bioeng Biotechnol 2015; 3: 162.
- Кветной И.М., Дробинцева А.О., Клейменова Т.С., Полякова В.О., Туркадзе К.А. Молекулярные механизмы замедления старения кожи под действием препарата плаценты человека. Молекулярная медицина 2019; 17(2): 50–55.

